
日本专利申请方式
1. 直接向JPO(日本特许厅)提出申请
2. 巴黎公约途径:在中国申请后,从中国申请日(即优先权日)起12个月内向JPO提出专利申请,可以享受优先权待遇。可以通过外语书面申请方式推迟4个月提交日语译文。
3. PCT途径:从国际申请的申请日(优先权日)起30个月内向JPO提出进入国家阶段的申请。可以在进入日起2个月内补交日语译文。
日本专利审查制度
1. 实审请求:任何人都可以在自日本申请日起3年内(巴黎公约途径)或自国际申请日起3年内(PCT途径)向JPO提出实审请求。
2. 加快审查制度
(1)加快审查:在实审请求的同时或之后可以提出加快审查。需满足的条件是①正在实施或准备实施的发明、或者②与外国申请相关的发明等。所需文件是情况说明书(包括现有技术检索结果及对比说明)。
(2)超级加快审查:在实审请求的同时或之后可以提出加快审查。需要同时满足①正在实施或准备实施的发明,②与外国申请相关的发明,以及③所有手续均为电子申请。除了现有技术检索结果及对比说明、还需提交实施情况说明。
(3)中日专利审查高速公路(PPH):在实审请求的同时或之后可以提出加快审查。需要同时满足①JPO申请具有至少一项被CNIPA认定为具有可专利性/可授权的权利要求,②JPO申请的所有权利要求必须与该可专利性权利要求充分对应,以及③JPO在申请人提出PPH请求之时尚未对申请进行审查。所需文件是权要求对应表、CNIPA认定为具有可专利性的所有权利要求副本及其译文、CNIPA就对应申请作出的所有审查意见通知书副本及其译文、CNIPA审查员引用的对比文献副本。
3. 修改限制
(1)主动修改:从申请到收到第一次OA之前均可进行主动修改,修改限制是不能增加未在原权利要求、说明书及附图中记载的内容。
(2)答复最初的审查意见通知书时的修改:答复期限为3个月,最多可延长3个月。修改限制是①不能增加未在原权利要求、说明书及附图中记载的内容;②被审查的发明与修改后的发明必须满足单一性的要求。
(3)答复最后的审查意见通知书时的修改:答复期限为3个月,最多可延长3个月。仅允许①删除权利要求;②权利要求范围的限定性缩减;③更正笔误;④对审查员指出不明确之处进行解释说明。
4. 分案申请:分案申请的时机是①允许修改的时期(主动修改、答复OA修改、提出复审请求同时的修改);②收到授权决定后30日内(前置审查中的授权决定除外);③收到最初的驳回决定后3个月(外国申请人4个月)内。
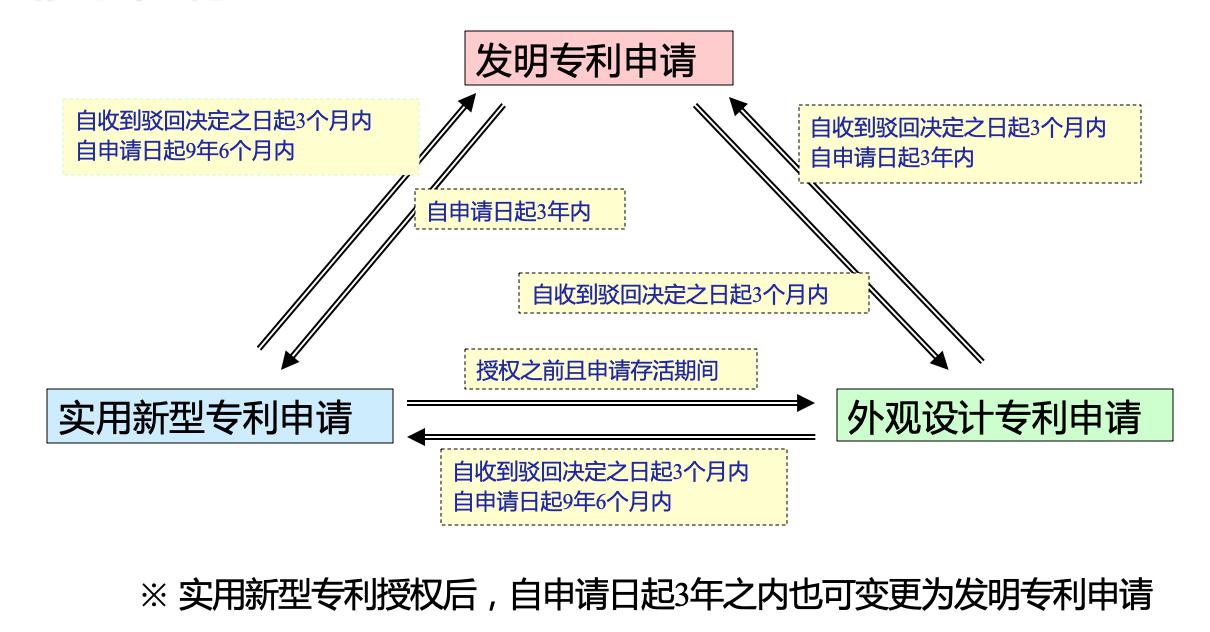
日本专利的变更申请制度
在一定条件内,发明、实用新型和外观设计专利申请可以互相变更。
日本专利的官费减免制度
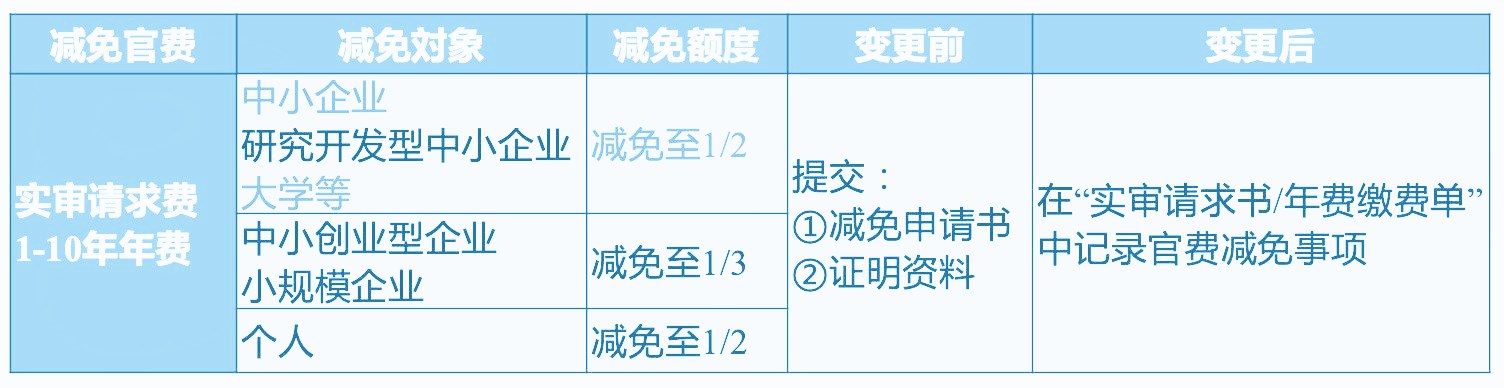
适用原则(具体是否适用需在申请前资讯日本代理人)
• 中小企业:判断基准根据企业的类型和领域而有所不同,制造型中小企业至少要满足①从业人员300人以下、②资本金3亿JPY以下
• 中小创业型企业:①成立不到10年,②资本金3亿JPY以下,③不受大企业支配。
• 个人:足各项收入总额小于250万JPY。
日本医药领域专利保护对象
人体的医疗方法(手术、治疗、诊断方法)不是专利保护对象。
医药领域专利保护对象包括:
• 医疗器械、药品等产品
• 医疗器械的工作方法(不包括医生的操作、器械对人体的作用过程)
• 从人体收集各种资料的方法(不包括判断病症以进行治疗):
• 处理从人体采集的样品的方法:
医药用途发明
定义:(i)发现某物质的未知属性,(ii)发现根据该属性,该物质可适用于新的医药用途。⇨属于产品发明
类型:①应用于特定疾病;②限定了给药时间、给药顺序、给药量、给药部位等用法用量的在特定疾病中的应用。
方法特征限定的产品权利要求(PBP权利要求)
1. 实审阶段规定:如果没有不可能/不现实事由导致无法直接用特性和结构限定物质X,PBP权利要求就是不明确(不清楚)的。
2. 被认定为“不明确”的PBP权利要求,处理方式如下:
① 删除该权利要求;
② 将该产品权利要求改为方法权利要求;
③ 删除该产品权利要求中的方法限定(改用结构、特性限定);
④ 说明不可能/不现实事由:物质结构或特性的解析在技术上是不可能的;或者确定物质结构或特性的操作需要庞大的经济支出或时间。
作者简介:
杨磊 专利代理人
关注我们
